Algunos tipos de epilepsia por causa demostrable tienen tratamiento específico, además del control de las crisis. Cuando la epilepsia es causada por una lesión no progresiva (secuelas de infarto cerebral, cisticercosis calcificada, etc.) o es genética, el tratamiento es el control de las crisis, además de la aplicación de cuidados generales y cambios de los hábitos de vida con la finalidad de evitar factores que puedan favorecer la presentación de las crisis.
Conducta ante una crisis
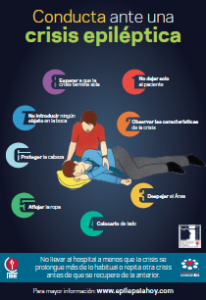
En caso de que el paciente presente crisis generalizadas tónicoclónicas es necesario explicar a la familia la conducta adecuada al momento de la crisis. Las recomendaciones son:
- No dejar solo al paciente, y observar las características de la crisis para informar posteriormente al médico.
2. Protegerlo, de lesiones colocándolo en un sitio seguro; es conveniente dejarlo en el piso, con una protección en la cabeza y lejos de escaleras o muebles con los que se pueda
3. Asegurar una buena oxigenación, aflojando la ropa y colocando la cabeza de lado para que la salivación excesiva y la acumulación de flemas salgan por un lado de la boca y no se obstruya la vía respiratoria.
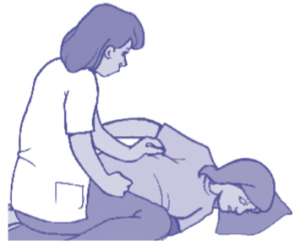
Gráfico 5. Atención de una crisis.
- No introducir ningún objeto en la boca, pues lejos de proteger la lengua puede lastimarse más a la persona y romperle los dientes, provocarle heridas en la boca o favorecer que trague parte del objeto que le puede obstruir la vía respiratoria o provocarle otras lesiones.
- Esperar que la crisis termine por sí misma, lo cual suele ocurrir en 2 a 5 minutos. Permitirle reposar en el periodo postictal. No llevarlo al hospital a menos que la crisis sea prolongada (más de 5 min.) o se repita antes de la recuperación de la conciencia. No aplicar medicamentos adicionales ni estímulos de ningún tipo. Registrar la crisis y continuar el tratamiento.
Calendario de crisis
Se recomienda al paciente y/o al familiar responsable de él, que anote las crisis día con día, cualquiera que sea el tipo de crisis lo cual permite tener un punto de comparación para evaluar los resultados del tratamiento.

Gráfico 6. Calendario para registro de crisis.
Medidas de higiene
Existen una serie de situaciones que no son causa de epilepsia pero sí actúan como factores que favorecen las crisis:
- Bebidas alcohólicas. Su ingesta abundante y prolongada puede provocar convulsiones en el periodo de deprivación. La asociación de bebidas alcohólicas con los medicamentos antiepilépticos aumenta los efectos tóxicos del alcohol y los efectos indeseables de los medicamentos.
- Actividad física. La respiración agitada favorece en algunos pacientes la presentación de sus descargas anormales y por tanto de crisis; sin embargo, esto ocurre cuando el paciente incrementa la frecuencia de sus respiraciones sin estar haciendo actividad física. El aumento de las respiraciones cuando se hace ejercicio es un mecanismo necesario de compensación para mantener la oxigenación del organismo ante el aumento de la actividad muscular y no suele provocar crisis. El grado de restricción dependerá de la edad, la actividad acostumbrada previamente por el paciente y su condición física. La práctica de cualquier deporte, incluyendo la natación, es permisible siempre y cuando se haga con vigilancia y sin llegar al agotamiento. La práctica de deportes de riesgo está restringida.
- Deprivación del sueño. Esta puede precipitar algunos tipos de crisis. Cuando el paciente requiera desvelarse por estudio o diversión se recomienda que duerma previamente una siesta y después del desvelo prolongue sus horas de sueño, teniendo mucho cuidado de continuar tomando puntualmente su medicina a la hora que le corresponde.
- Ayuno prolongado. La disminución severa de glucosa (azúcar) en la sangre puede provocar crisis convulsivas aún en sujetos que no padecen epilepsia. Es suficiente con que el paciente haga sus comidas a las horas usuales sin excederse en cantidad y/o frecuencia.
- Interacciones medicamentosas. Algunos medicamentos que pudieran requerirse para tratar otras enfermedades que se pueden presentar en cualquier persona, como una diarrea, una gripa, etc., elevan los niveles de los medicamentos antiepilépticos y pueden provocar manifestaciones de intoxicación, mientras que otros los disminuyen y ocasionan descontrol de la epilepsia. El médico debe conocer estas interacciones para elegir el medicamento más apropiado. Nunca se debe suspender el tratamiento antiepiléptico porque se requiera un tratamiento adicional de manera transitoria.
- Suspensión del medicamento. La interrupción brusca del tratamiento por la razón que sea, puede ocasionar un estado epiléptico, que es muy peligroso, pues ocurren crisis continuas durante tiempo prolongado. Cualquier modificación de dosis se debe realizar muy lentamente y si se va a cambiar un medicamento por otro, es necesario hacerlo lentamente también.
Elección y uso de los medicamentos antiepilepticos
No existe un medicamento ideal. Los fármacos o medicamentos antiepilépticos de que se dispone en la actualidad, bien utilizados, pueden lograr un buen control de la epilepsia hasta en el 80% de los casos. Los lineamientos generales de un buen tratamiento antiepiléptico son los siguientes:
- Elegir el medicamento adecuado para el tipo de crisis. No todos son igualmente útiles para todas las crisis.
- Iniciar el tratamiento con un solo medicamento. Esto permite saber a qué atribuir tanto los efectos benéficos como los indeseables.
- Prescribirlo a la dosis adecuada por kg de peso/día en los niños y de acuerdo a la dosis promedio recomendada en adultos. Para evitar efectos colaterales dependientes de dosis, se debe incrementar gradualmente la cantidad en varios días o semanas según el medicamento, hasta alcanzar la dosis planeada.
- Repartir las tomas del medicamento en el horario adecuado, de acuerdo a la vida media del medicamento (vida media es el tiempo que tarda un medicamento en ser eliminado del organismo a la mitad de su concentración), con horario exacto marcado en el reloj: cada 24 hs, cada 12 hs, cada 8 hs, de acuerdo a las características de cada medicamento.
- Esperar el tiempo suficiente para que el fármaco alcance su estabilidad en la circulación (estado estable), que ocurre al transcurrir cinco vidas medias antes de decidir si es o no el adecuado.
- Hacer niveles séricos (análisis de sangre que mide la concentración del medicamento) una vez transcurrido el periodo para lograr el estado estable; esto es un auxiliar, y siempre debe correlacionarse con la condición clínica del paciente. No hay niveles séricos accesibles para todos los medicamentos y muchos de los de nueva generación no los requieren porque la concentración es directamente proporcional a la dosis,
- Mantener el tratamiento por tiempo suficiente. Una vez logrado un control al 100%, el tratamiento debe continuar SIN CAMBIOS por un periodo no menor de 4 años después de la última crisis por «pequeña» que sea, antes de pensar en su posible retiro. Si se toma esta decisión tras la re-evaluación del caso y la toma de un nuevo EEG que debe estar normal, la reducción paulatina debe llevar por lo menos 6 meses adicionales.
| Tabla 6. Fármacos antiepilépticos y sus indicaciones | |
| Fármacos clásicos | Fármacos nuevos |
| Fenobarbital1 | Oxcarbazepina1 |
| Fenitoína1 | Vigabatrina1,4 |
| Primidona1 | Gabapentina1 |
| Carbamazepina1 | Lamotrigina1,2,3,4,5 |
| Valproatos1,2,3,4,5 | Topiramato1,2,3,4,5 |
| Benzodiazepinas (clonazepam, clobazam)2,4,5 | Levetiracetam1,2,3,4,5 |
| Pregabalina1 | |
| Lacosamida1 | |
| 1CPS, CPC,CGTC, 2Atónicas, 3Ausencias, 4Espasmos infantiles, 5Mioclónicas | |
Características de los medicamentos antiepilépticos
El tratamiento de la epilepsia con medicamentos se inició en el siglo XIX, con la utilización de los bromuros. Desde entonces, a los largo de los años se han desarrollado diversos fármacos que son actualmente de uso común, y se encuentran otros más en investigación. Cualquiera que sea el medicamento, sufre un proceso en el organismo que empieza con su absorción en el tubo digestivo; pasa a la circulación y se distribuye en todos los tejidos del organismo, realiza su acción en el cerebro y sufre modificaciones en el hígado hasta su eliminación. Cuando se ha eliminado la mitad de la cantidad del fármaco circulante en un momento dado, se denomina vida media, concepto de suma importancia para determinar el horario de la toma de la medicación.
Al igual que cualquier medicamento, los fármacos antiepilépticos tienen efectos colaterales que en ocasiones son severos y pueden obligar a descontinuar el tratamiento.
La mayoría de los medicamentos antiepilépticos interactúan entre sí, por lo que es recomendable evitar asociaciones. Ocasionalmente éstas pueden intentarse y en esos casos es necesario tener en mente los efectos recíprocos sobre los respectivos niveles.
Con los fármacos antiepilépticos conocidos es posible controlar satisfactoriamente cerca del 80% de los casos de epilepsia, lo cual no siempre se logra con el primer tratamiento elegido.
Como mencionamos en los lineamientos generales, lo más recomendable es la monoterapia (terapia con un solo medicamento), pues con las asociaciones de medicamentos se presentan interacciones y es difícil saber a cuál droga atribuir tanto los efectos terapéuticos como los indeseables.
La medición de los niveles séricos de los fármacos antiepilépticos es un auxiliar valioso. Al inicio de un tratamiento sirven como una guía para ajustar dosis siempre y cuando se realicen pasado el tiempo necesario para alcanzar el estado estable (cinco vidas medias, cuando los niveles del fármaco circulante tienen mínimas variaciones). Si el paciente se controla bien y no hay manifestaciones colaterales es innecesario repetir los niveles periódicamente, pero si no hay buen control o hay efectos colaterales o tóxicos es conveniente hacerlos para decidir las modificaciones pertinentes.
Fármacos tradicionales
Los llamados fármacos tradicionales son aquéllos que tienen en uso varias décadas y cuyos efectos tanto terapéuticos como colaterales y tóxicos son ya muy bien conocidos: fenobarbital, fenitoína, primidona, carbamazepina, valproatos y benzodiazepinas, de los que se describirán sus indicaciones y efectos colaterales.
Fenobarbital. Se introdujo en 1912 como inductor de sueño y tranquilizante, pero se descubrió por Hauptmann ese mismo año que las crisis epilépticas tenían una marcada reducción con su uso.
Indicaciones: crisis tónicoclónicas generalizadas y crisis parciales.
Efectos colaterales y tóxicos: sedación, ataxia (desequilibrio al caminar), mareo, insomnio, hiperquinesia (actividad excesiva), cambios del talante (estado de ánimo), agresividad, disfunción cognitiva (alteración de funciones intelectuales), impotencia, reducción de la libido (impulso sexual), deficiencia de folato, de vitamina K y D, osteomalacia (descalcificación de los huesos), hombro congelado, anormalidades del tejido conectivo, erupciones de la piel.
A pesar de los efectos colaterales, es muy efectivo y barato. Muchos de los efectos son dependientes de dosis, por lo que una vigilancia adecuada, con la dosis mínima efectiva, mejora la tolerabilidad.
Fenitoína. En 1938 se descubrió el efecto antiepiléptico de la fenitoína sin efecto hipnótico (efecto productor de sueño), lo cual significó un cambio muy notable en el tratamiento de la epilepsia, hasta entonces a base de bromuros y fenobarbital y fue el primer producto que mostró efectividad antiepiléptica en animales antes de ser probado en seres humanos.
Indicaciones: crisis focales y crisis generalizadas tónico-clónicas.
Efectos colaterales y tóxicos: ataxia (desequilibrio al caminar), mareo, letargia (sueño excesivo), sedación, dolor de cabeza, disquinesia (movimientos anormales), cambios de talante, depresión, agresión, neuropatía periférica (afectación de los nervios o “cables” que transmiten la sensibilidad desde la piel y los impulsos para el movimiento de los músculos); hipersensibilidad (reacción alérgica manifestada por erupción cutánea, fiebre, anemia entre otras); deficiencia de folatos, anemia megaloblástica, afectación de la médula ósea (tejido que se encuentra en el interior de los huesos y que produce los elementos de la sangre); hepatitis, deficiencia de vitamina K, defectos de coagulación; disminución de las inmunoglobulinas (proteínas que constituyen los anticuerpos o defensas del organismo), descalcificación, disfunción tiroidea, disfunción hormonal, pérdida de la libido, trastornos del tejido conectivo, pseudolinfoma (crecimiento no canceroso de los ganglios), vasculitis (inflamación de arterias), miopatía (afectación de los músculos que produce debilidad); rasgos faciales toscos, hirsutismo (exceso de vello corporal), hinchazón de las encías.
Carbamazepina. A finales de los años 50 se probó exitosamente como antiepiléptico y como tratamiento de la neuralgia del trigémino, estableciéndose en los siguientes años como uno de los antiepilépticos más importantes del mundo.
Indicaciones: crisis parciales y crisis generalizadas tónico-clónicas.
Efectos colaterales y tóxicos: somnolencia, fatiga, mareo, ataxia (desequilibrio al caminar), diplopía (visión doble), visión borrosa, reacciones cutáneas, discrasias de médula ósea (falla en la producción de los elementos de la sangre: glóbulos rojos, glóbulos blancos o plaquetas), hiponatremia (disminución del nivel de sodio), retención de agua y nefritis.
Valproato. B.S. Baron lo sintetizó por primera vez en 1882 y fue usado inicialmente como un solvente orgánico. Meunier, en 1963, fue el primero que identificó su acción antiepiléptica mientras lo usaba como solvente en el tamizaje de nuevas drogas antiepilépticas. Los primeros estudios clínicos fueron reportados por Carraz en 1964 y desde entonces su uso ha sido cada vez más difundido. Del ácido valproico se han derivado el valproato de magnesio, el valproato de sodio y el divalproato de sodio.
Indicaciones: Crisis parciales y todo tipo de crisis generalizadas (tónico-clónicas, ausencias, mioclonías, atónicas).
Efectos colaterales y tóxicos: hepatitis severa en niños pequeños (efecto raro), pancreatitis, insuficiencia renal, mareo, trastornos intelectuales, agresividad, temblor, debilidad, encefalopatía (estado de confusión mental), disminución de plaquetas, disminución de glóbulos blancos, anemia, adelgazamiento y pérdida del cabello, ganancia de peso.
| Tabla 7. Fármacos tradicionales: dosis | |||
| Nombre | Siglas | mg/kg | Dosis promedio |
| Fenobarbital | PB | 3-5 | 50-200 |
| Fenitoína | PHT | 4-7 | 100-300 |
| Primidona | PMD | 5-20 | 250-750 |
| Carbamazepina | CBZ | 15-30 | 600-1800 |
| Valproato | VPA | 20-60 | 600-2400 |
| Tabla 8. Fármacos | |
| FAE clásicos | Efectos adversos principales |
| Fenobarbital, primidona | Hiperquinesia en niños, irritabilidad, limitación del desarrollo psicomotor |
|
Fenitoína |
Desmineralización ósea, cuadro parecido a lupus o a linfoma, inflamación de las encías, deformidad de rasgos faciales, aumento del vello corporal |
|
Carbamazepina |
Ronchas, anemia, disminución de glóbulos rojos, blancos y plaquetas, disminución del sodio circulante |
| Benzodiazepinas | Efectos opuestos a los esperados |
|
Valproatos |
Temblor, confusión mental, ganancia de peso, ovarios poliquísticos, caída del cabello |
Fármacos nuevos disponibles en México
Todos han sido producto de investigaciones encaminadas a encontrar tratamientos antiepilépticos y han sido ensayados primero en animales y luego en seres humanos antes de su comercialización. Las indicaciones iniciales para los primeros ensayos clínicos son crisis parciales simples o complejas con o sin generalización secundaria, de difícil control, en pacientes mayores de 14 años. Para su evaluación de eficacia y tolerabilidad se han comparado con carbamazepina o fenitoína y se considera como medida de eficacia la reducción de crisis igual o mayor al 50% en relación a la frecuencia basal, todos utilizados como terapia de adición al esquema de tratamiento que previamente tenía el paciente. La mayoría han sido ensayados ya en niños y en síndromes epilépticos como el Lennox-Gastaut, encontrándose otras indicaciones para algunos de ellos. Igualmente se han ensayado como tratamiento único en epilepsia de reciente inicio. A continuación nos referiremos a cada uno de los que tenemos disponibles en México.
Oxcarbazepina. Es tan efectiva como la carbamazepina y tiene sus mismas indicaciones pero es mejor tolerada, los efectos indeseables son similares a los de la carbamazepina, pero ocurren con menor frecuencia sobre todo en cuanto a las reacciones cutáneas.
Felbamato. Fue sintetizado por los laboratorios Wallace en 1954.
Indicaciones: Terapia coadyuvante en epilepsia parcial y generalizada refractarias y en el síndrome de Lennox-Gastaut.
Efectos colaterales y tóxicos: trastorno severo del hígado y anemia aplástica (daño en la médula ósea, donde se producen todos los elementos de la sangre) son los más serios, aunque raros. Otros son: insomnio, pérdida de peso, síntomas gastrointestinales, fatiga, mareo, letargia, cambios de conducta, ataxia, trastornos visuales, cambios del estado de ánimo, reacción psicótica y erupciones en la piel. Se ha retirado la aprobación de la Food and Drug Adminstration (FDA) de EUA para su uso, debido a los efectos adversos graves
Lamotrigina. En vista de que varios de los antiepilépticos tradicionales tienen efectos antifolato (reducen una vitamina llamada ácido fólico), se consideró que esto era una propiedad anticonvulsiva y la investigación en ese sentido por parte de laboratorios Wellcome dio como resultado la producción de feniltriazinas, de las que derivó la lamotrigina, una triazina de estructura química diferente a la de otros antiepilépticos. Su acción antifolato es muy débil, pero su efecto antiepiléptico es muy bueno, por lo que ambos efectos se consideran independientes en la actualidad.
Indicada en todos los tipos de crisis.
Efectos colaterales y tóxicos: erupción cutánea que puede llegar a una extrema gravedad llamada síndrome de Stevens Johnson, dolor de cabeza, anemia, ataxia, astenia, diplopía, náusea, vómito, mareo, somnolencia, insomnio, depresión, psicosis y aumento de crisis.
Vigabatrina. El GABA (Ácido Gama Amino Butírico) es la sustancia frenadora del sistema nervioso central y sus anomalías se relacionaron con la presentación de epilepsia, motivo por el que muchas investigaciones se encaminaron por este rumbo y se originó la vigabatrina, que es un compuesto parecido al GABA.
Indicaciones: Terapia coadyuvante en la epilepsia parcial y generalizada refractarias, así como en el síndrome de West y el síndrome de Lennox-Gastaut.
Efectos colaterales y tóxicos: sedación, mareo, cefalea, ataxia (pérdida del equilibrio), parestesias (sensaciones raras), agitación, amnesia, cambios del ánimo, depresión, psicosis, confusión, agresividad, ganancia de peso, diarrea, trastornos del campo visual por daño en la retina.
Gabapentina. Indicaciones: Terapia coadyuvante en epilepsias parcial y generalizada refractarias.
Efectos indeseables y tóxicos: somnolencia, mareo, ataxia, somnolencia, cefalea, temblor diplopía, náusea, vómito, rinitis y aumento de crisis.
Topiramato. Tiene varios mecanismos de acción.
Indicaciones: Indicado en todo tipo de crisis menos las ausencias.
Efectos colaterales y tóxicos: mareo, ataxia, cefalea, parestesias, temblor, somnolencia, trastornos cognitivos, confusión, agitación, amnesia, depresión, labilidad emocional, náusea, diarrea y pérdida de peso.
Levetiracetam. Tiene una absorción rápida y casi completa, su vida media es de 6 a 8 horas. Está indicado para crisis parciales con o sin generalización secundaria y tiene potencial en varios tipos de crisis generalizadas. Se utiliza a dosis de 1000 a 3000 mg al día dividido en dos tomas con buena tolerabilidad y eficacia.
Efectos adversos: somnolencia, astenia, mareo, irritabilidad.
Pregabalina. El nombre químico de la pregabalina es [(S)-3-(aminometil)-5- ácido metilhexanoíco; CI-1008], un ligando alfa -2-delta(a2d). La alfa -2-delta es una proteína auxiliar asociada con los canales de calcio voltaje dependientes. La pregabalina bloquea fuertemente a la subunidad a2d ocasionando una reducción de la entrada de calcio a las terminaciones nerviosas y reducción de la liberación de varios neurotransmisores como glutamato, noradrenalina, serotonina, dopamina y la sustancia P. Está indicada para crisis focales con o sin generalización secundaria, su presentación es en cápsulas de 75 y 150 mg y se administra c/12 hs. No se une a proteínas, se elimina por vía renal y sus efectos adversos son: aumento del apetito e Incremento de peso; somnolencia, mareo, euforia, confusión, disminución de la libido, irritabilidad, ataxia, alteración en la atención, incorrdinación, alteración en la memoria, temblor, disartria, parestesias, visión borrosa, diplopia, vertigo, sequedad de boca, constipación, vómitos, flatulencia, disfuncion eréctil, fatiga, edema periferico.
Lacosamida. Actúa reforzando selectivamente la inactivación lenta de los canales de sodio y uniéndose a la proteína 2 mediadora de respuesta a colapsina (CRM P-2) (aunque este mecanismo no se sabe cómo actúa en la epilepsia). Viene en presentaciones de tabletas de 50 mg, 100 mg, 150 mg y 200 mg y en ampolletas de 200 mg/20 ml. Puede administrarse con alimentos, biodisponibilidad de casi el 100%, unión a proteínas en 15%, eliminación predominantemente renal. Dosis promedio: 200 a 400 mg por día en dos tomas. Indicado en crisis focales con o sin generalización secundaria. Efectos adversos: mareo, cefalea. Precaución en pacientes con problemas conocidos de la conducción cardiaca o tomando drogas que prolongan el intervalo PR o con enfermedad cardiaca severa, en quienes se debe tomar electrocardiograma (EKG) antes de iniciar y al alcanzar el estado estable.
Como acabamos de ver, existen muchos fármacos para el tratamiento de la epilepsia, por lo que no es aceptable que se mantenga por años un tratamiento que no logra la meta del control total, ya que hay muchas otras opciones que se pueden ensayar, elegidas apropiadamente de acuerdo al tipo de crisis, la edad del (la) paciente y desde luego, la disponibilidad del medicamento y su costo.
Se pretende que esta revisión permita una mejor elección, pero nunca la automedicación. Siempre debe ser el médico quien decida cuál fármaco y cómo administrarlo, de acuerdo a las características de cada medicamento y de cada paciente. El tratamiento siempre debe ser individualizado y a la medida de cada quien, a la dosis apropiada, horario adecuado y tiempo suficiente. Resumimos las dosis en la Tabla 9 y los efectos adversos más frecuentes de los fármacos nuevos en la Tabla 10.
| Tabla 9. Presentaciones y dosis de los antiepilépticos nuevos | |||
|
Presentación |
mg/kg/día niños | mg/día adultos | |
| Oxcarbazepina | Tabs. 300 y 600 mg | 10-30 | 600-1200 |
| Felbamato | Tabs. 400 mg, Susp. 600 mg/5 ml | 15-45 | 2400-3600 |
| Vigabatrina | Tabs. 500 mg | 40-80 | 1000-1500 |
| Lamotrigina | Tabs. 25 y 100 mg | 5-15 | 200-400 |
| Gabapentina | Cáps. 300 y 400 mg | 15-30 | 900-3600 |
| Topiramato | Tabs. 25 y 100 mg | 3-6 | 100-200 |
| Levetiracetam | Tabs. 500 y 1000 mg | 15-45 | 1000-3000 |
| Pregabalina | Cáps. 75 y 150 mg | 3-10 | 150-600 mg |
| Lacosamida | Tabs. 50, 100, 150, 200 mg | 5-15 | 200-400 |
| Tabla 10. Efectos adversos de los fármacos nuevos | |
| FAE nuevos | Efectos adversos |
| Lamotrigina | Reacción alérgica (Stevens Johnson), insomnio, sensación de excesiva alerta |
| Felbamato | Anemia aplástica |
| Vigabatrina | Retinopatía, reducción de campos visuales |
|
Topiramato |
Reducción de peso, dificultad para encontrar las palabras, sensación de adormecimiento en las extremidades, cálculos renales |
| Levetiracetam | Irritabilidad, psicosis |
| Lacosamida | Mareo, síncope, depresión |